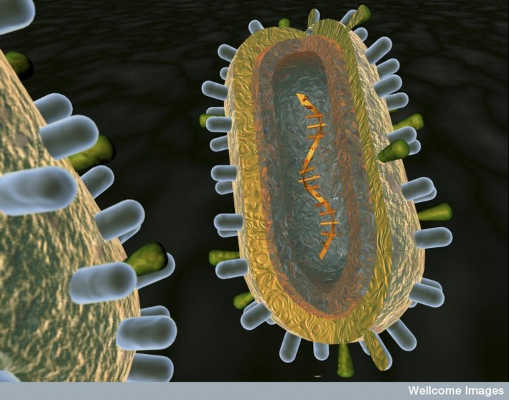
 הצגה של האמן באנטומיה של וירוס. אנה טאנצוס/תמונות וולקום, CC BY-NC-ND
הצגה של האמן באנטומיה של וירוס. אנה טאנצוס/תמונות וולקום, CC BY-NC-ND
אף אחד לא רוצה לחלות בשפעת, וקו ההגנה הטוב ביותר הוא החיסון העונתי לשפעת. אך ייצור זריקת שפעת שנתית יעילה מסתמך על חיזוי מדויק של אילו זני שפעת צפויים להדביק את האוכלוסייה בכל עונה נתונה. זה דורש תיאום של מרכזי בריאות מרובים ברחבי העולם כשהנגיף עובר מאזור לאזור. ברגע שאפידמיולוגים מסתדרים על זני שפעת המטרה, ייצור החיסונים עובר להילוך גבוה; זה לוקח כשישה חודשים לייצר יותר מ -150 מיליון מנות להזרקה הכרחית לאוכלוסייה האמריקאית.
עד כמה פועל החיסון השנתי נגד שפעת?
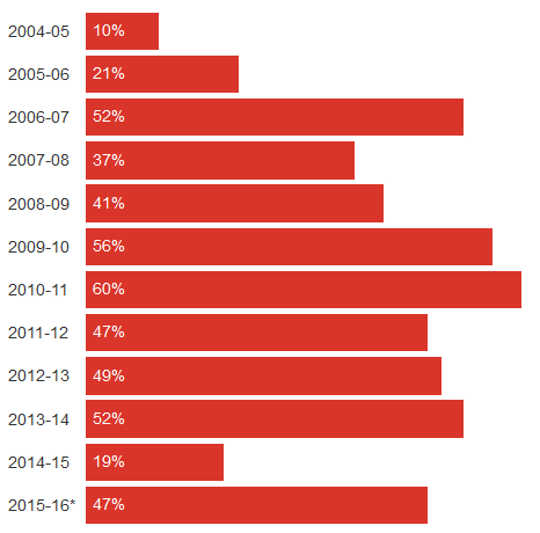
ייצור זריקת שפעת שנתית אפקטיבית מסתמך על חיזוי מדויק של אילו זני שפעת צפויים להדביק את האוכלוסייה בעונה נתונה. ה- CDC מבצע מדי שנה מחקרי תצפית לחישוב "יעילות החיסון" לצילום של אותה שנה.
לחיזוי אפידמיולוגי לא נכון או שלם יכולות להיות השלכות גדולות. בשנת 2009, בעוד יצרנים, כולל MedImmune וסאנופי פסטר, היו מכינים חיסונים נגד הזנים הצפויים, א זן שפעת נוסף, H1N1, הגיח. החיסון המוכן לא הגן מפני זן בלתי צפוי זה, וגרם לפאניקה עולמית ולמעלה מ -18,000 מקרי מוות מאושרים - כנראה רק חלק קטן מהמספר האמיתי, מוערך בכ -150,000 אלף. מוטב מאוחר מאשר לעולם לא, בסופו של דבר הופק חיסון נגד H1N1, הדורש זריקה נוספת של שפעת באותה שנה.
בהתחשב בכך שפעת גרמה לרוב מגפות במהלך 100 השנים האחרונות - כולל שפעת 1918 כי הביאו לכ -50 מיליון מקרי מוות - נשארנו עם השאלה: האם מדענים יכולים לייצר חיסון "אוניברסלי" המסוגל להגן מפני זני שפעת מגוונים, כזה שאינו דורש תחזיות שנתיות של אפידמיולוגים וזריקה שנתית עבורך?
חיסונים מעודדים את מערכת החיסון להילחם
עד המאה ה -18, וניתן לטעון שהרבה יותר מוקדם בהיסטוריה, היה ידוע כי א ניצול אבעבועות שחורות לא היה יורד מזה שוב בחשיפה שלאחר מכן. איכשהו, זיהום העניק חסינות כנגד המחלה. ואנשים זיהו שחלבניות שבאו במגע עם בקר רדוף באבעבועות הפרה יהיו מוגנות באופן דומה מפני אבעבועות שחורות.
בסוף 1700, חקלאי בנימין ג'סטי חיסן את משפחתו באבעבועות פרה, למעשה לחסן אותם מפני אבעבועות שחורות, למרות החשיפה העתידית. רוֹפֵא אדוארד ג'נר הזניק אז את האנושות לעידן חדש של אימונולוגיה כאשר נתן אמון מדעי בהליך.
אז אם חיסון אחד של אבעבועות פרה או חשיפה אחת (והישרדות של) אבעבועות רוח מעניק חסינות בשווי של עשור או אפילו לכל החיים, מדוע מעודדים אנשים לקבל את החיסון נגד שפעת מדי שנה?
התשובה טמונה באיזו מהירות האנטומיה של נגיף השפעת משתנה. כל וירוס מורכב מממברנה כדורית בערך הכוללת חומר גנטי המשתנה כל הזמן. קרום זה מתובל בשני סוגים של "קוצים": המגלוטינין, או HA, ונויראמינידאז, או NA, שכל אחד מהם מורכב מגבעול וראש. HA ו- NA מסייעים לנגיף בזיהום על ידי קישור לתאים המארחים, ומתווכים את כניסת הנגיף לתא ולבסוף יציאתו.
חיסונים בדרך כלל מעוררים נוגדנים המכוונים לשתי המולקולות הללו. לאחר הזריקה, המערכת החיסונית של האדם מתחילה לפעול. תאים מיוחדים אוספים את מולקולות החיסון כפולשים; תאים אחרים יוצרים אז נוגדנים שיזהו את המולקולות הזרות. בפעם הבאה שאותם פולשים יופיעו - בין אם בצורה של אותו חיסון ובין אם זני הנגיף שהוא מחקה - תאי החיסון של הגוף מזהים אותם ונלחמים בהם ומונעים זיהום.
עבור מפתחי חיסונים, מאפיין מתסכל אחד לגבי הגנום המוטה של שפעת הוא כמה מהר HA ו- NA משתנים. השינויים הקבועים האלה הם אלה שמחזירים אותם ללוח הציור לחיסונים חדשים בכל עונת שפעת.
שיטות שונות לעיצוב חיסון
חיסון האבעבועות השחורות היה הראשון שהשתמש ב"פרדיגמה האמפירית "של החיסונים - אותה אסטרטגיה בה אנו משתמשים במידה רבה כיום. הוא מסתמך על גישת ניסוי וטעייה כדי לחקות את החסינות הנגרמת כתוצאה מזיהום טבעי.
במילים אחרות, מפתחי החיסונים מאמינים שהגוף יעלה תגובת נוגדנים למשהו בחיסון. אבל הם לא מתמקדים באיזה תיקון ספציפי של הנגיף גורם לתגובה חיסונית. זה לא ממש משנה אם זו תגובה לתיקון קטן של HA שזנים רבים חולקים, למשל. כאשר משתמשים בנגיף שלם כחומר מוצא, אפשר לקבל נוגדנים רבים ושונים המזהים חלקים רבים ושונים של הנגיף המשמש בחיסון.
זריקת השפעת העונתית מתאימה בדרך כלל לגישה אמפירית זו. בכל שנה, האפידמיולוגים צופים אילו זני שפעת הם הסבירים ביותר להדביק אוכלוסיות, בדרך כלל מתיישבים על שלושה או ארבעה. החוקרים לאחר מכן מחלישים או משביתים זנים אלה כדי שיוכלו לפעול כמחקים בחיסון לשפעת של אותה שנה מבלי לתת לנמענים את השפעת המלאה. התקווה היא שמערכת החיסון של הפרט תגיב לחיסון על ידי יצירת נוגדנים המכוונים לזנים אלה; ואז כשהוא יבוא במגע עם שפעת, הנוגדנים יחכו לנטרל את הזנים האלה.
אבל יש דרך אחרת לעצב חיסון. זה נקרא עיצוב רציונלי ומייצג שינוי פרדיגמה שיכול לשנות את המשחק בחיסונים.
המטרה היא לעצב מולקולה כלשהי - או "אימונוגן" - שיכולה לגרום לייצור נוגדנים יעילים ללא צורך בחשיפה לנגיף. ביחס לחיסונים הנוכחיים, האימונוגן המהונדס עשוי אף לאפשר תגובות ספציפיות יותר, כלומר התגובה החיסונית מכוונת לחלקים מסוימים של הנגיף, ולרוחב גדול יותר, כלומר הוא יכול להתייחס לזנים מרובים או אפילו וירוסים קשורים.
אסטרטגיה זו פועלת למקד אפיטופים ספציפיים, או תיקונים של הנגיף. מכיוון שנוגדנים פועלים על ידי זיהוי מבנים, המעצבים רוצים להדגיש בפני המערכת החיסונית את התכונות המבניות של החיסונים שהם יצרו. אז חוקרים יכולים לנסות לתכנן חיסונים מועמדים עם מבנים אלה בתקווה שהם יעוררו את המערכת החיסונית לייצר נוגדנים רלוונטיים. דרך זו עשויה לאפשר להם להרכיב חיסון המעורר תגובה חיסונית יעילה ויעילה יותר מהאפשר בשיטת ניסוי וטעייה המסורתית.
התקדמות מבטיחה התקדמה עיצוב חיסון לנגיף סינציאלי נשימתי באמצעות הפרדיגמה הרציונלית החדשה הזו, אך עדיין נמשכים מאמצים להשתמש בגישה זו לשפעת.
לקראת חיסון אוניברסלי נגד שפעת
בשנים האחרונות חוקרים בודדו מספר נוגדנים חזקים, המנטרלים אינפלונזה המיוצרים בגופנו. בעוד תגובת הנוגדן לשפעת היא מכוון בעיקר לראשו של ספייק HA, כמה נמצאו כי הגבעול של HA. מכיוון שהגזע קבוע יותר על פני זנים ויראליים מאשר הראש, ייתכן שזו עקב אכילס של שפעת, ונוגדנים המכוונים לאזור זה עשויים להיות תבנית טובה לעיצוב חיסונים.
חוקרים נוקטים במספר גישות שיכולות לגרום לגוף לייצר נוגדנים מעניינים אלה לפני שהוא נדבק. אסטרטגיה אחת, המכונה תצוגת ננו -חלקיקים, כוללת עיצוב מולקולה המשלבת חלק מהנגיף. במעבדה, מדענים יכלו לצרף שילוב כלשהו של חלקיקי HA ו- NA לחלקיק החיצוני של חלקיקי כדור אשר עצמו מסוגל לגרום לתגובה חיסונית. כאשר הוא מוזרק כחלק מחיסון, המערכת החיסונית יכולה "לראות" את המולקולות הללו, ובמזל לייצר נגדן נוגדנים.
אחת השאלות העיקריות שצריך לענות עליהן היא מה בדיוק צריך להיות מוצג בחלק החיצוני של חלקיקים אלה. חלק מהאסטרטגיות מציגות גרסאות שונות של מולקולות HA מלאות, בעוד שאחרות כוללות רק גבעולים. בעוד שצריך לאסוף נתונים נוספים על בני אדם כדי לאמת גישות אלה, הנתונים ממחקרים בבעלי חיים משתמשים בהם אימונוגנים גזעיים בלבד מעודדים.
עם הטכנולוגיה הנוכחית, יתכן שלעולם לא תהיה זריקה נגד שפעת "אחת וסיימה". ומעקב אפידמיולוגי תמיד יהיה הכרחי. עם זאת, לא מן הנמנע שנוכל לעבור ממודל של פעם בשנה לגישה של אחת לעשר שנים, וייתכן שאנחנו נמצאים בתוך שנים ספורות בלבד לאחר שהיינו שם.
![]()
על המחבר
איאן סתליף, דוקטורט. סטודנט, תוכנית בביולוגיה כימית ופיזית, מרכז החיסונים ואנדרבילט, האוניברסיטה ונדרבילט ואמין מורג'י, דוקטורט. סטודנט, המחלקה למיקרוביולוגיה ואימונולוגיה, מרכז החיסונים ואנדרבילט, האוניברסיטה ונדרבילט
מאמר זה פורסם במקור ב שיחה. קרא את מאמר מקורי.
ספרים קשורים:
at InnerSelf Market ואמזון